標題:Personal Neoantigen Vaccines Induce Persistent Memory T Cell Responses and Epitope Spreading in Patients with Melanoma
期刊:Nat Med
影響因子:53.44
導讀
借助單細胞測序技術我們可以對一些腫瘤治療方法的療效進行評估,例如個人新抗原疫苗被認為是誘導、放大和多樣化抗腫瘤 T 細胞反應的有效方法。8 位曾接受過手術的黑色素瘤治療的患者疾病復發,對他們應用疫苗治療并評估其臨床療效與引起的循環免疫反應。這幾位患者接受 Neo Vax 的治療時長中位數為 4 年,這是一種長肽鏈疫苗,平均為每個病人靶向 20 個針對其自身腫瘤的新抗原。所有患者均存活,其中 6 例無活躍疾病癥狀。實驗人員觀察到疫苗接種后新抗原特異性 T 細胞反應的長期持久性,體外檢測能夠找到記憶表型的新抗原特異性 T 細胞。隨著時間的推移,新抗原特異性 T 細胞克隆多樣化,隨之出現多種 T 細胞受體克隆型,顯示出不同的功能親和性。此外,他們檢測到疫苗接種和抗原表位擴散后新抗原特異性 T 細胞克隆腫瘤浸潤的證據,提示靶向疫苗誘導腫瘤殺傷。因此,個人新抗原肽疫苗誘導的 T 細胞應答持續多年并且能拓寬黑色素瘤患者的腫瘤特異性細胞毒性范圍。
科學問題
個性化定制的疫苗在持續數年的腫瘤治療中效果如何?
實驗設計
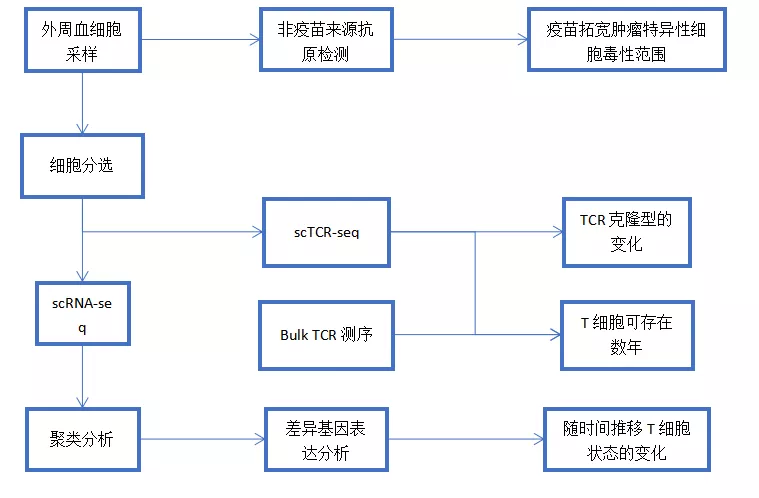
8 位高風險黑色素瘤復發患者在整個療程中取自不同時間節點的外周血細胞。
技術平臺
10X genomics
1、疫苗誘導的新抗原特異性 CD4+ T 細胞表現出記憶和細胞毒性特征
為驗證疫苗的療效機制,實驗人員首先著手確定在注射后患者體內疫苗誘導的新抗原特異性 T 細胞演化流程。為此他們對每位患者免疫新抗原的 T 細胞轉錄特征進行評估,聚焦于新抗原免疫的 CD4+ T 細胞的分離與辨認。被成功分離且在一系列時間節點上數據可用的樣本共有 4 個,實驗證明在這些 PBMC 樣品中 CD4+ T 細胞能夠在體外被檢測到(從第三周開始接種疫苗,持續整個療程)(圖 1a,b)。對這 4 名病人中的 3 位進行單細胞測序,在合并所有的細胞并聚類后,共定義出 4 個細胞類群(圖 1d)。對每個聚類的顯著基因進行評估,發現每個不同的 T 細胞狀態都由特定的基因標記辨別(圖 1d,e)。為了確定疫苗接種的特定階段是否與不同的轉錄狀態相關,實驗人員根據轉錄識別簇評估每個時間點的組成(圖 1d,f)。在接種前樣本中分離出來的 CD4+ T 細胞主要表現為“幼稚樣”T 細胞表型(cluster 0)。在開始治療與加強針注射后(8-20 周)分離出來的 T 細胞主要存在于 cluster1,2 中,揭示了在注射治療過程中 T 細胞有關細胞毒性和淋巴細胞凋亡樣(AICD)狀態的轉變(圖 1g)。在經歷一次加強針注射的 4 周后大多數被分選出的 T 細胞表現出記憶樣表型。綜上,實驗結果闡述了在接種新抗原特異性疫苗后 T 細胞從幼稚到效應,凋亡,到記憶分化狀態的明顯轉變。
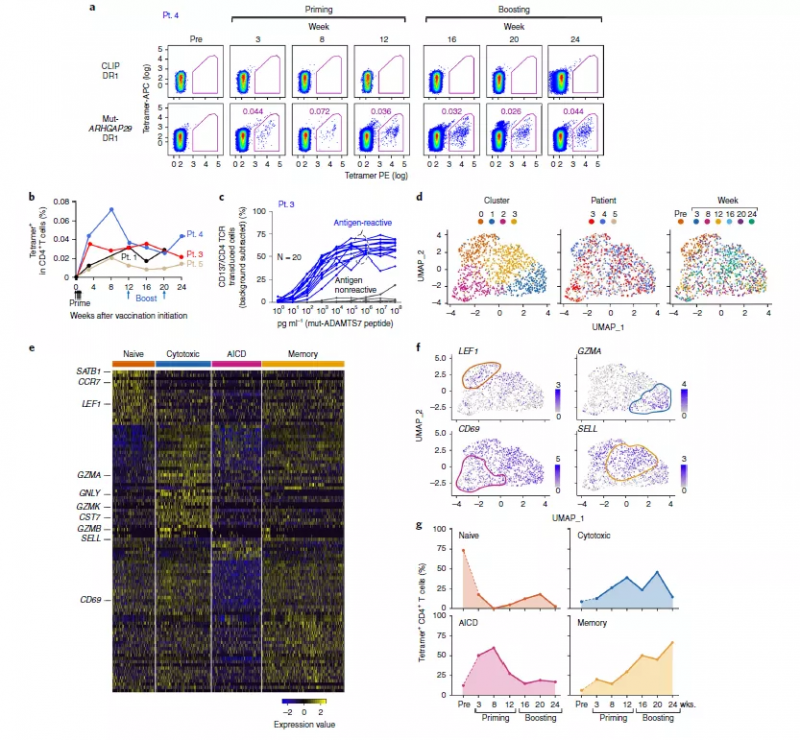
圖 1 新抗原特異性 T 細胞在疫苗接療程中的轉錄譜
2、在接種疫苗和抗 PD- 1 治療后,新抗原特異性 TCR 克隆型多樣化
為確定在整個疫苗療程中新抗原特異性 T 細胞的克隆組成轉變,研究人員也對這 3 位病人的 TCR 圖譜進行了評估。在接受疫苗注射(3,8,12 周)后和加強針注射(16,20,24 周)后能夠觀察到新克隆型的多種 T 細胞迅速出現(圖 2)。他們也評估了 2 和 6 號病人在注射疫苗并進行派姆單抗治療后的新抗原特異性 T 細胞圖譜多樣性。對于這兩名患者,經歷疫苗注射和派姆單抗治療后在第 16 周經過一輪體外刺激,可以檢測到靶向新抗原的 CD4+ T 細胞群(圖 3a)。2 號病人的 TCR 克隆型分析顯示,在 16 周檢測到的 99 個(25%)mut-adm2 特異性 TCR 克隆型中,25 個(25%) 在派姆單抗治療啟動后大約一年后的 89 周仍然存在;值得注意的是,15 個克隆型中有 13 個(87%) 被證實為抗原反應型(圖 3b)。在第 16 周出現的 10 個主要克隆型中,有 5 個仍然存在于派姆單抗治療一年后觀察到的 10 個主要克隆型中,在派姆單抗啟動一年后 10 個主要的克隆型中有 9 個在第 16 周中就已經存在(圖 3C)。在第 16 周時,10 個主要的克隆型中有 9 個仍然在派姆單抗啟動一年后觀察到的 10 個主要克隆型中,所有出現在派姆單抗處理一年后的 10 個主要的克隆在第 16 周就已經存在(圖 3C)。總之,這些種群動態表明,在抗 PD- 1 治療后,TCR 克隆型會呈現出大量維持以及新克隆型的出現會使 TCR 庫發生轉變。
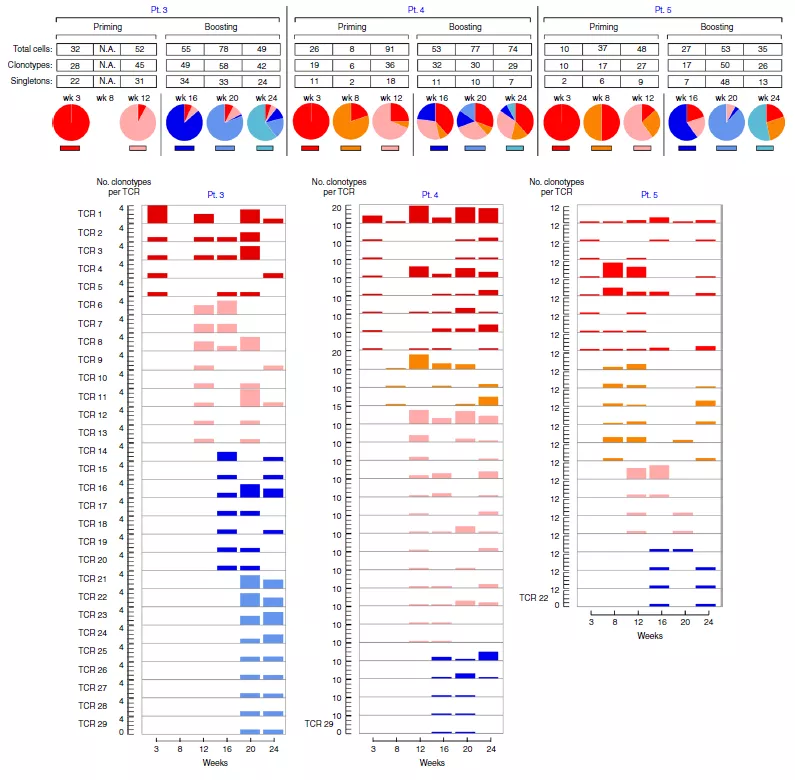
圖 2 新抗原特異性 T 細胞的 TCR 圖譜動力學
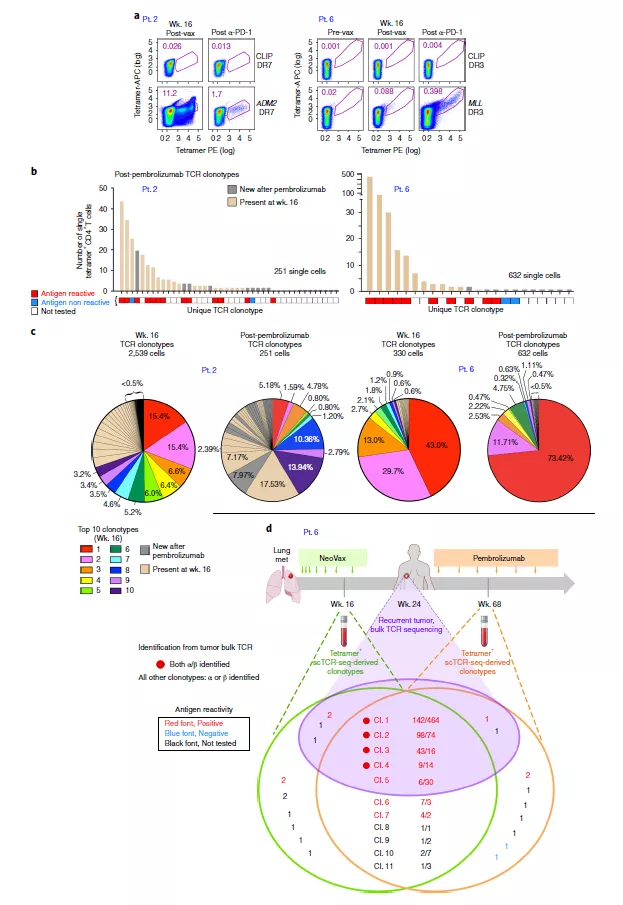
圖 3 在疫苗注射和 PD- 1 抑制后新型抗原特異性 TCR 動力學
3、個人新抗原疫苗誘導產生持續數年的記憶 T 細胞反應和 TCR 克隆型
為了評估疫苗誘導的新抗原特異性 T 細胞的長期持久性,實驗人員使用開始接種疫苗后 28 至 55 個月收集的 PBMC 樣本檢測 T 細胞應答情況。結果表明,在疫苗注射的 4.5 年后 T 細胞對曾經免疫處理過的大多數多肽仍能做出響應(圖 4a)。在長時間節點上都保留有可利用的 bulk TCR 測序數據的樣本中,他們檢測到了 7 個同樣被單細胞 TCR 測序在治療初期和強化針注射階段找到的 TCRα/ β 對(圖 4c),在克隆水平上證明了疫苗誘導的 T 細胞在接種疫苗后還能存活數年。
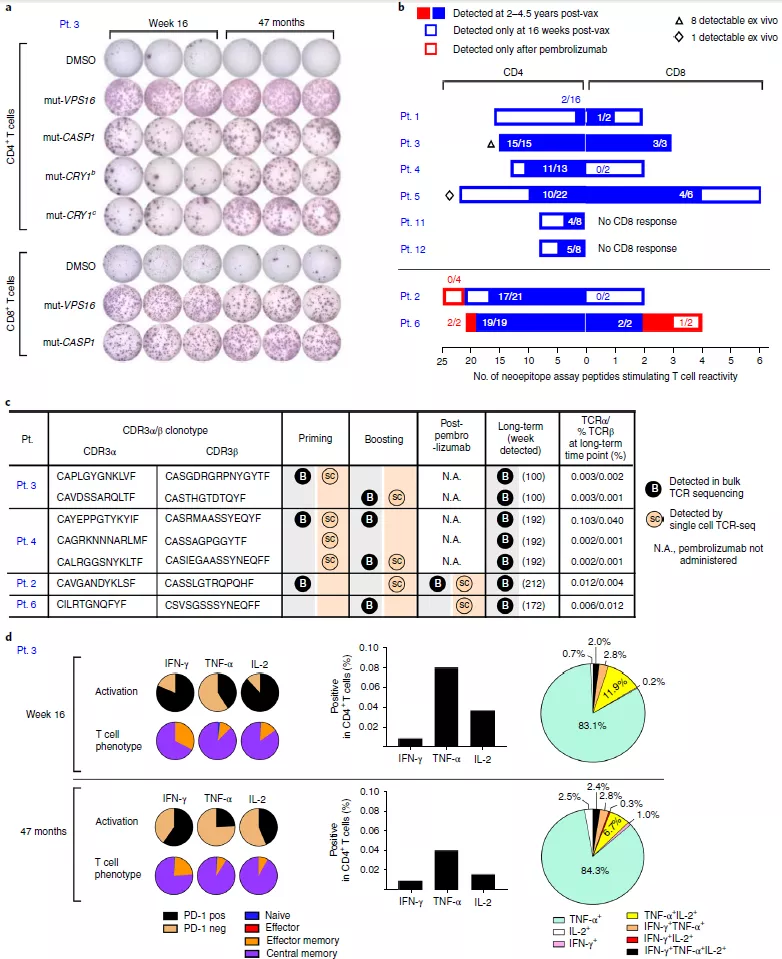
圖 4 疫苗誘導的新抗原特異性 T 細胞能夠存活數年
4、個人新抗原疫苗誘導 T 細胞反應的表位擴散,提示腫瘤細胞溶解
由于無法對患者直接評估疫苗介導的抗腫瘤效果,考慮到腫瘤的破壞會釋放出新的腫瘤相關抗原(TAA),因此實驗人員針對這些擴散開的額外抗原進行檢測(圖 5a)。對于 3 號病人他們共檢測出 2 個非疫苗來源的新抗原(mut-EYA3 和 mut-P2RY4)(圖 5b)。對于 2 號和 6 號病人,他們在 2 號病人體內檢測出了 mut-AGAP3c,MAGEF,mut-AGAP3b 和 MAGED 4 個抗原(圖 5c),而 6 號病人體內未觀察到非疫苗肽的應答。對于 2,3 號病人,他們分別觀察到 CD4+ T 細胞對已識別的非疫苗新抗原的持續應答持續到接種疫苗后 4.5 年和 4 年(圖 5d)。總之,上述數據顯示,在接種疫苗后早期可檢測到表位擴散,在抗 PD - 1 治療后可擴展到其他靶點,并持續數年。
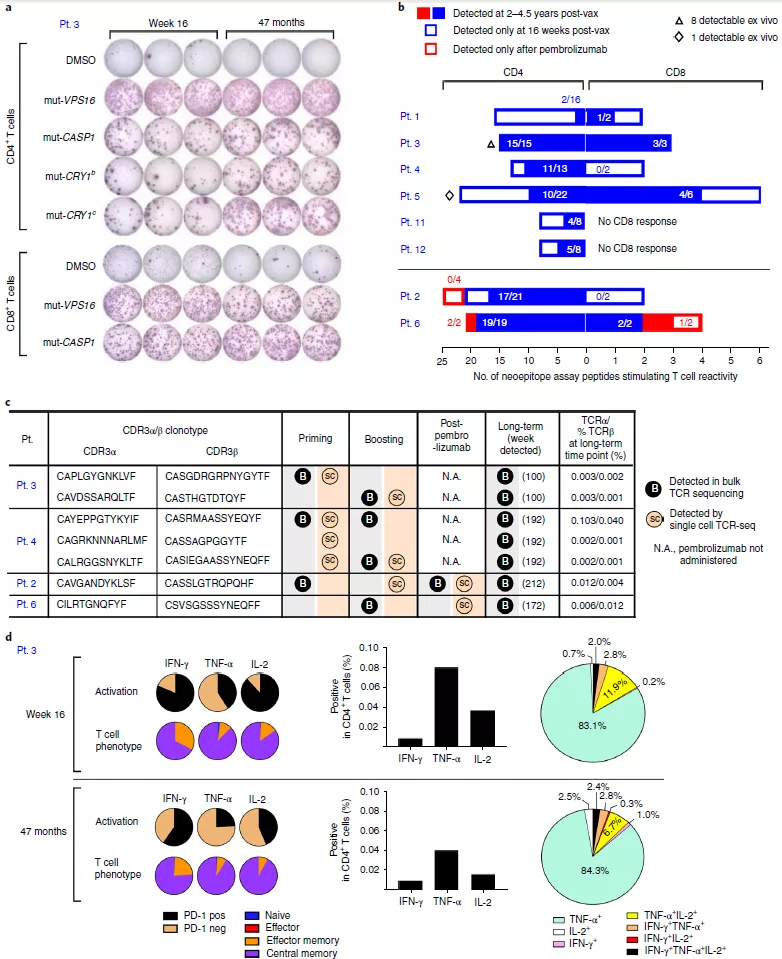
圖 5 疫苗誘導的 T 細胞反應擴散到非疫苗新抗原和 TAA 表位
參考文獻:
[1].Hu Z, Leet DE, Alles?e RL, Oliveira G, Li S, Luoma AM, Liu J, Forman J, Huang T, Iorgulescu JB, Holden R, Sarkizova S, Gohil SH, Redd RA, Sun J, Elagina L, Giobbie-Hurder A, Zhang W, Peter L, Ciantra Z, Rodig S, Olive O, Shetty K, Pyrdol J, Uduman M, Lee PC, Bachireddy P, Buchbinder EI, Yoon CH, Neuberg D, Pentelute BL, Hacohen N, Livak KJ, Shukla SA, Olsen LR, Barouch DH, Wucherpfennig KW, Fritsch EF, Keskin DB, Wu CJ, Ott PA. Personal neoantigen vaccines induce persistent memory T cell responses and epitope spreading in patients with melanoma. Nat Med. 2021 Mar;27(3):515-525. doi: 10.1038/s41591-020-01206-4. Epub 2021 Jan 21. PMID: 33479501; PMCID: PMC8273876.

